‘
Men verwacht dat de nieuwe techniek bij
meer dan 75% van de onoplosbare patiën-
ten de erfelijke oorzaak kan vinden.
’
19
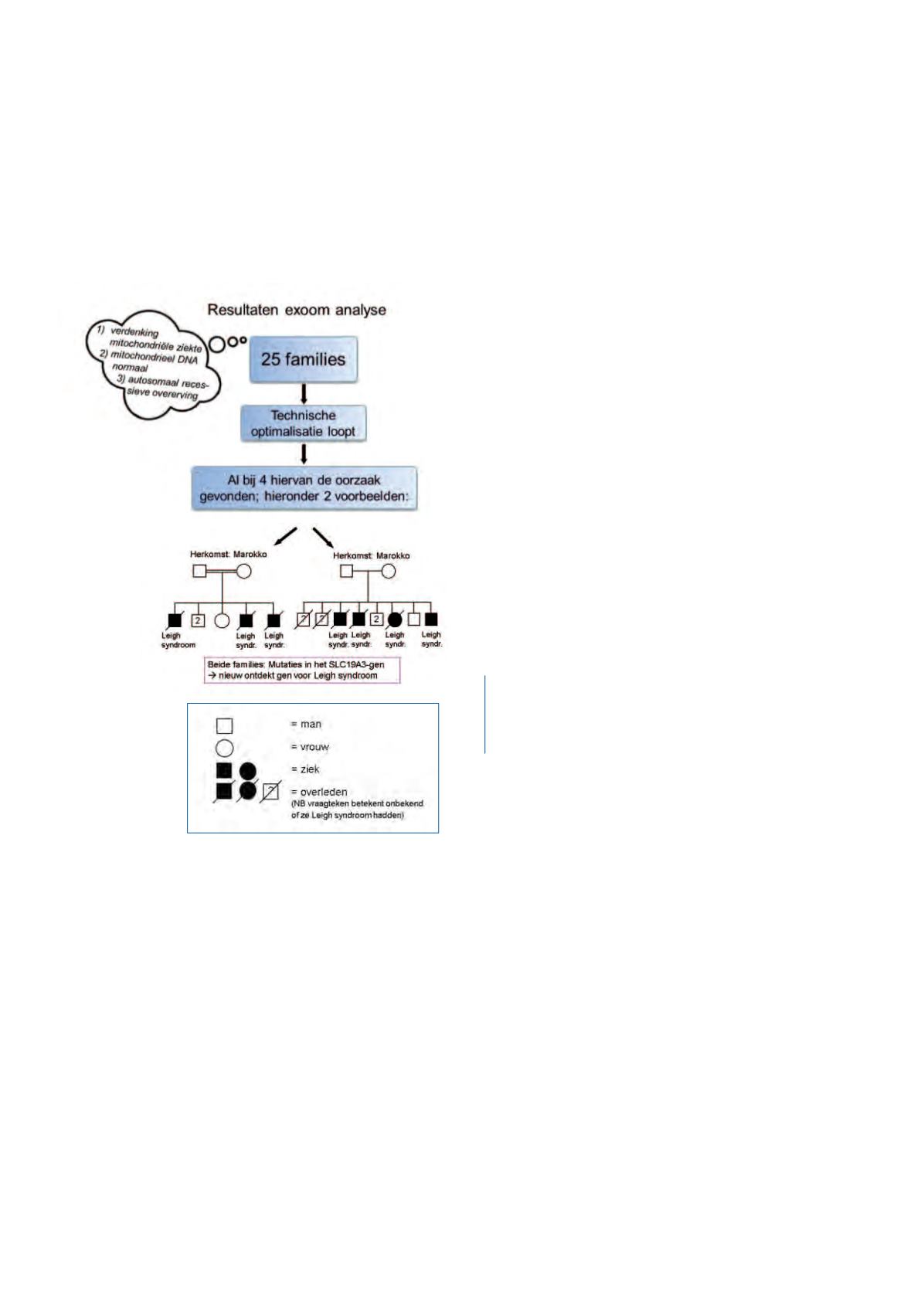
rzaak van mitochondriële ziekten
Van opsporing tot behandeling
Daarnaast is het ook mogelijk om alle genen in één keer te
onderzoeken. Dit wordt ook wel exoom-analyse genoemd.
Bij steeds meer families is gestart met deze uitgebreide
screening. Het speuren in de genen is in volle gang. Het zoe-
ken van een groot aantal genen levert veel DNA-variaties per
patiënt op. Maar lang niet alle variaties hebben iets te bete-
kenen. Door het wegstrepen van variaties die (waarschijnlijk)
geen betekenis hebben, houdt men uiteindelijk een aantal
mogelijke oorzaken over. Vervolgens zoekt men verder naar
dat ene gen die de ziekte veroorzaakt. Bij vier families is dit
gen inmiddels gevonden en bij een groot aantal andere
families komt de uitslag dichterbij. Als voorbeeld zijn de
stambomen van twee families met hetzelfde afwijkende gen
te zien in bovenstaand figuur. Er bleek dat deze afwijking op-
merkelijk vaak aanwezig is bij patiënten die uit een bepaald
deel van Marokko komen. Bovendien lijken deze patiënten
baat te hebben bij een hoge dosis thiamine of biotine. Deze
informatie kan essentieel zijn bij de ontwikkeling van een mo-
gelijke therapie. Dit voorbeeld laat zien dat het vinden van de
genetische oorzaak ook nieuwe inzichten kan bieden in een
mogelijke behandeling.
Advies
Wanneer alle genen worden onderzocht, kunnen afwijk-
ingen gevonden worden die niet met de mitochondriële
ziekte te maken hebben. Het is daarom belangrijk om de
patiënt en/of de ouders vooraf hier goed over te informeren.
Daarnaast speelt genetisch advies ook een belangrijke rol
voor ouders met een kinderwens en een eerder kind met
een mitochondriële aandoening. Zij stellen vaak de vraag
hoe ze kunnen voorkomen dat zij opnieuw een ziek kind
krijgen. Ook is hierbij het vinden van het gen dat de ziekte
veroorzaakt van groot belang. Wanneer de genetische
afwijking bekend is, zijn er mogelijkheden om een kind te
krijgen zonder de mitochondriële ziekte. Verschillende
onderzoeken, zoals prenatale diagnostiek of preïmplantatie
genetische diagnostiek (PGD), kunnen hierbij helpen. Bij pre-
natale diagnostiek wordt DNA-onderzoek uitgevoerd bij
het ongeboren kind tijdens de zwangerschap. PGD is
embryoselectie en kan in Nederland alleen uitgevoerd
worden in het Maastricht UMC in samenwerking met het
UMC Utrecht en UMC Groningen (
.
Verwachting
Men verwacht dat de nieuwe techniek bij meer dan 75% van
de onoplosbare patiënten de erfelijke oorzaak kan vinden.
Daarnaast zal de manier waarop een genetische afwijking
tot een ziekte leidt ook beter zichtbaar worden. Dit kan in
een aantal gevallen direct leiden tot behandelingsopties voor
deze ernstige aandoeningen. Daarnaast geeft kennis over
de genetische afwijking ouders ook de mogelijkheid om te
voorkomen dat zij (nog) een kind met de ziekte krijgen. Het
onderzoek naar nieuwe genen, die betrokken zijn bij mito-
chondriële ziekten, betreft een samenwerkingsverband tus-
sen de afdeling Klinische Genetica van het Academisch
Ziekenhuis Maastricht (Maastricht UMC+) en de afdeling
Neurologie van het Erasmus MC in Rotterdam. Deze nieuwe
DNA-techniek vergroot de kans op het vinden van de erfe-
lijke oorzaak enorm.
Suzanne Sallevelt, klinisch geneticus i.o. (Maastricht UMC+)
René de Coo, (kinder-) neuroloog (ErasmusMC)
Bert Smeets, professor in Klinische Genoomanalyse met als
aandachtsgebied de mitochondriële ziektes (MUMC+)


